Sputnik V tem aspectos de biossegurança aprovados por órgão técnico
Imunizante ainda precisa de aval da Anvisa para ser aplicado no Brasil
A Comissão Técnica Nacional de Biossegurança (CTNBio) aprovou requisitos de biossegurança da vacina Sputnik V, desenvolvida pelo Instituto russo Gamaleya em parceria com a farmacêutica brasileira União Química.
A aprovação da CTNBio é condição para a inserção de qualquer organismo geneticamente modificado no mercado brasileiro, a exemplo de vacinas como a Sputinik V. Contudo, o uso do imunizante depende de aprovação também da Agência Nacional de Vigilância Sanitária. A análise da Agência teve início na tarde desta segunda-feira (26).
Segundo a CTNBIo, órgão ligado ao Ministério da Ciência, Tecnologia e Inovações (MCTI), a análise das informações teve início na semana passada. Foram solicitados documentos adicionais à União Química, como informações sobre o método de obtenção de linhagens de adenovírus.
A União Química entregou à CTNBio a documentação exigida. Os integrantes da Comissão entenderam que os dados complementares atenderam às exigências necessárias para a aprovação.
De acordo com a comissão, a aprovação dos aspectos de biossegurança é passo importante para o processo de avaliação e eventual permissão da importação e ou do registro definitivo da vacina.
Importação
A Diretoria Colegiada da Anvisa delibera na noite desta segunda-feira o pedido de governadores para a importação em caráter especial de doses da Sputnik V. Essa solicitação não consiste no registro completo e definitivo, mas se baseia na legislação atual voltada para medidas de combate à pandemia, que abre a possibilidade da importação de imunizantes autorizados por órgãos sanitários de uma série de países.
Já a aprovação da CTNBio faz parte das exigências feitas para imunizantes que lidem com organismos geneticamente modificados. Mas a aprovação da CTNBio não é suficiente para a viabilização da importação, do registro em caráter emergencial ou do registro definitivo.
 CÂNCER GRÁVIDA DESCOBRE CÂNCER AVANÇADO E ANTECIPA PARTO PARA SALVAR BEBÊ E COMEÇAR O TRATAMENTO EM GOIÂNIA
CÂNCER GRÁVIDA DESCOBRE CÂNCER AVANÇADO E ANTECIPA PARTO PARA SALVAR BEBÊ E COMEÇAR O TRATAMENTO EM GOIÂNIA 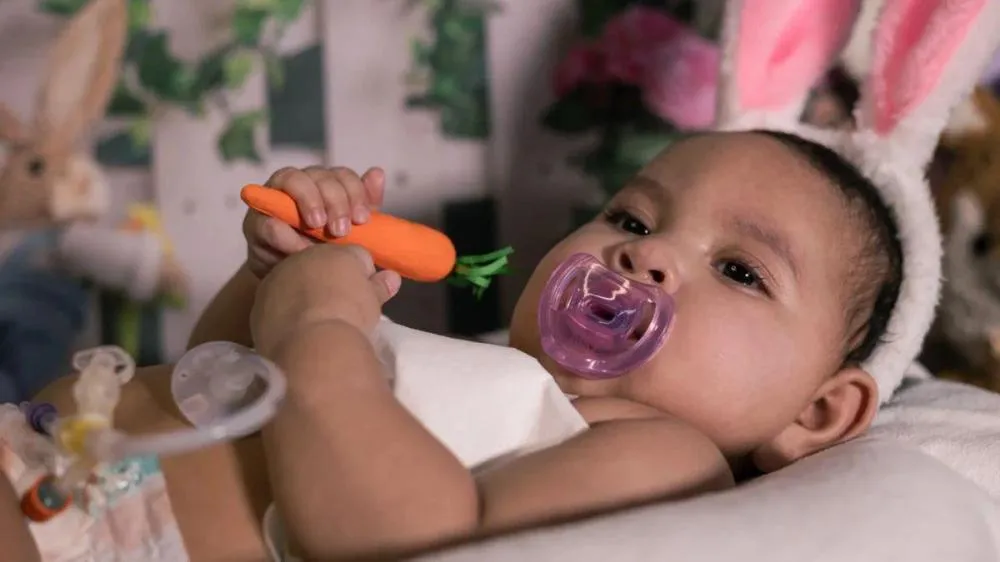 PÁSCOA Ensaio fotográfico de Páscoa leva cor e esperança para crianças em UTI de Goiânia
PÁSCOA Ensaio fotográfico de Páscoa leva cor e esperança para crianças em UTI de Goiânia  Afastamento Conheça as novas regras da licença-maternidade após internação
Afastamento Conheça as novas regras da licença-maternidade após internação  Inclusão Projetos que beneficiam pessoas com Transtorno do Espectro Autista passam na Câmara de Goiânia
Inclusão Projetos que beneficiam pessoas com Transtorno do Espectro Autista passam na Câmara de Goiânia 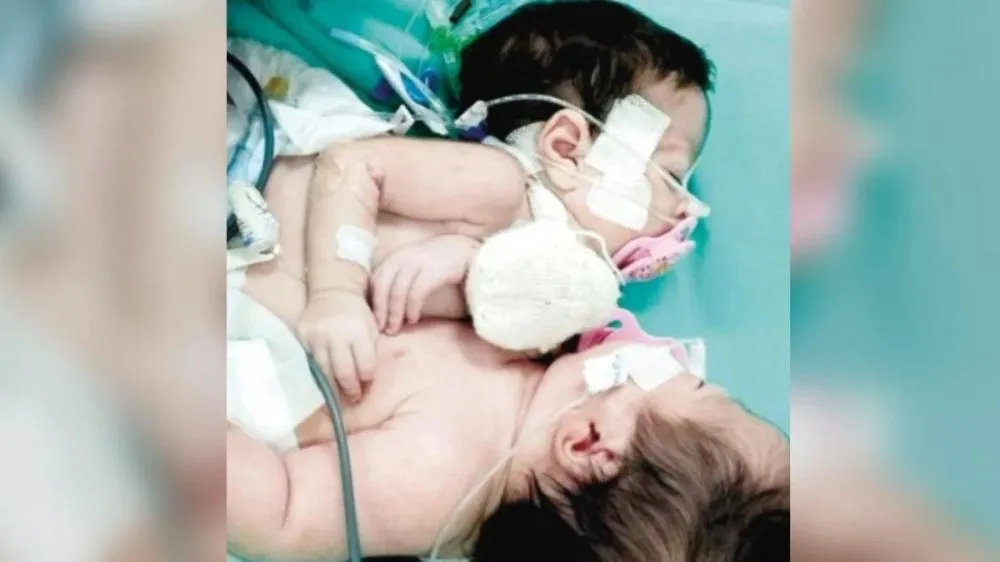 Boa Notícia Siamesas de Manaus recebem alta da UTI, em Goiânia
Boa Notícia Siamesas de Manaus recebem alta da UTI, em Goiânia  Saúde 7 alimentos que ajudam a dormir melhor (sem pesar na consciência!)
Saúde 7 alimentos que ajudam a dormir melhor (sem pesar na consciência!) Mín. 21° Máx. 28°
Mín. 19° Máx. 29°
Chuvas esparsasMín. 19° Máx. 28°
Chuva Concursos e Emprego Concursos GO 2026: vagas abertas e previstas em Goiás
Concursos e Emprego Concursos GO 2026: vagas abertas e previstas em Goiás  Bastidores da Política Combustíveis: Petrobras nega defasagem nos preços e reforça sua política de reajustes
Bastidores da Política Combustíveis: Petrobras nega defasagem nos preços e reforça sua política de reajustes  Tecnologia e Games Jogos do PS Plus Essential de abril são revelados! Confira a lista completa
Tecnologia e Games Jogos do PS Plus Essential de abril são revelados! Confira a lista completa  'Fui um babaca', diz Arthur sobre querer conhecer amigas de Viih Tube
'Fui um babaca', diz Arthur sobre querer conhecer amigas de Viih Tube 



